引言
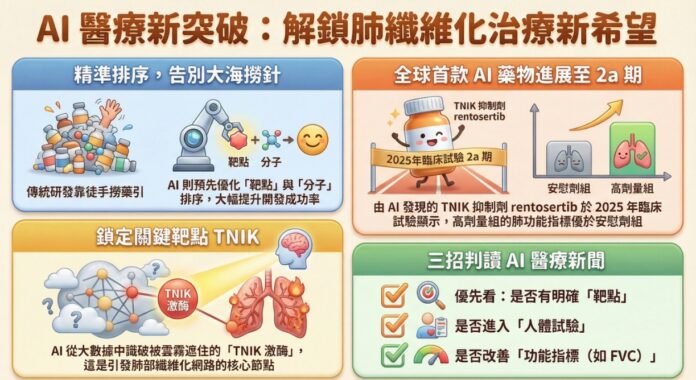
當一種病被寫成「原因不明」,最沉重的,往往不是那四個字,而是病人和家屬接下來那種不知道該往哪裡走的感覺。你可能也有這種感覺:醫療明明一直在進步,可一碰到某些肺病,還是常聽到「先控制看看」。你以為新藥研發最難的是找到有效成分,其實更難的,常常是先看見真正該打的那個點。特發性肺纖維化多年來一直是難治疾病,很多治療只能拖慢惡化,卻很難真正改變病程。現在,AI藥物研發開始把這件事往前推了一步。2025 年發表的臨床試驗顯示,AI 找出的 TNIK 抑制劑 rentosertib 已走到 Phase 2a,且高劑量組的肺功能指標變化優於安慰劑組(註1)。這不只是「AI 很厲害」的故事,而是醫學開始學會在混亂裡更早看見機轉、選對分子,再把希望慢慢帶進人體試驗。這篇文章想陪你看懂的,就是這條新路究竟改變了什麼,離病人的生活又還有多遠。
引言參考文獻:
- (註1) Xu Z, Ren F, Wang P, et al. A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine. 2025. Nature Medicine (nature.com)
- Ren F, Aliper A, Chen J, et al. A small-molecule TNIK inhibitor targets fibrosis in preclinical and clinical models. Nature Biotechnology. 2025. Nature Biotechnology (nature.com)
AI藥物研發跟傳統新藥開發,到底差在哪裡?
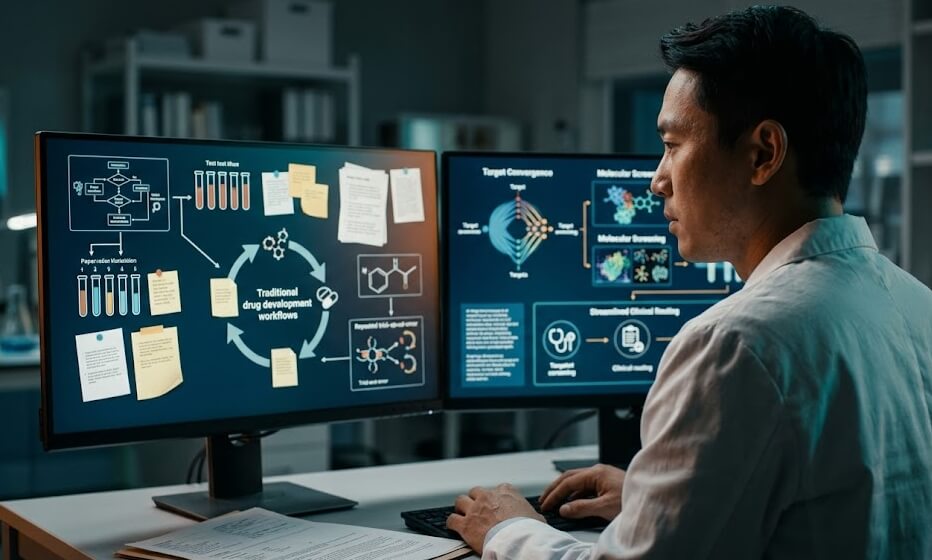
傳統新藥開發,常像在一大鍋藥材湯裡徒手撈出那一味真正有用的藥引,時間長、成本高,還常常撈到最後才發現方向不對。AI藥物研發不一樣,它不是替科學家按下捷徑鍵,而是先幫忙把「哪個靶點最值得追、哪個小分子最可能成功」這件事做更早、更精準的排序。近年的研究指出,AI已能參與治療標的探索、分子設計與前期篩選;在特發性肺纖維化(IPF)這類路徑複雜、過去轉譯困難的疾病上,研究團隊便以AI辨識出TNIK,並推進到小分子候選藥與人體試驗,這代表改變的不只是速度,而是整條研發路徑的判讀方式。(註1)(註2) 不過,別把 AI Drug Discovery 想成萬能鑰匙。模型再聰明,也仍受限於資料品質、偏差與可解釋性;換句話說,AI 能幫你把火候抓得更準,卻不能替你省略真正下鍋試煮的那一步。

特發性肺纖維化為什麼這麼難治?AI 又為什麼特別有機會切進來?
特發性肺纖維化不是單純「肺變硬」而已,它更像一鍋早已悶燒許久的濃湯,表面看起來只是咳、喘、肺功能下降,底下其實牽動的是發炎、修復失衡、纖維母細胞活化與細胞外基質堆積等多條路徑一起失控。也因為如此,IPF 長年最難的,不只是找藥,而是找出哪一個節點才是真正值得攻的地方。你可能也有這種感覺:醫學明明進步很快,為什麼遇到某些病,還是常聽到「原因不明」?其實關鍵就在這裡。當疾病不是單一路徑,而是一整張交錯網路時,AI 藥物研發的優勢才會浮現。近年的回顧指出,AI 在 IPF 的應用不只限於影像判讀,還延伸到整合臨床、形態學與多組學資料,幫助研究者更早辨識高價值標靶與可能受益的治療方向;而 2025 年的 Phase 2a 試驗也讓 rentosertib 成為一個具體例子,證明 AI 不只是會「看見問題」,而是可能真的把候選新藥往臨床推進一步。(註3)(註4) 當然,這仍不代表 IPF 已被攻克,因為再漂亮的模型,最後都得回到真實病人身上接受時間與安全性的考驗。
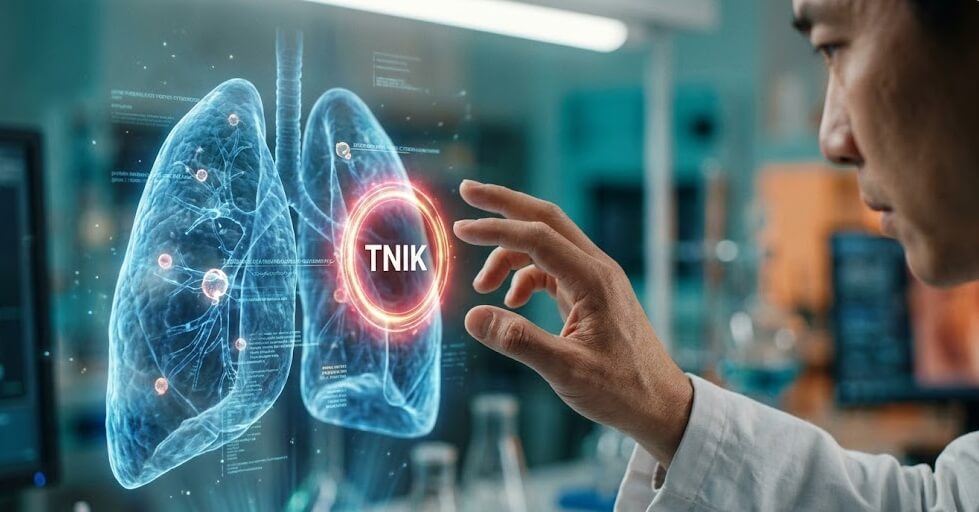
TNIK 跟 rentosertib 是什麼?AI 是怎麼把新藥一步步找出來的?
如果把傳統藥物研發比作在山林裡摸黑找路,那麼 TNIK 的出現,像是研究者終於在地圖上看見一座原本被霧遮住的山頭。TNIK 是一個和纖維化訊號網路密切相關的激酶,研究團隊先用 AI 從大量疾病資料裡辨識出它,再往下設計、篩選並優化小分子,最後做出 rentosertib,也就是先前稱為 ISM001-055 的候選藥物。這一步很關鍵,因為 AI 藥物研發真正厲害的地方,不只是把分子生得更快,而是能把「哪個分子值得被做進去」這件事提早判斷。2025 年發表的研究顯示,rentosertib 已進入隨機、雙盲、安慰劑對照的 Phase 2a 試驗,且高劑量組在用力肺活量變化上優於安慰劑組,安全性表現也具可接受性。 但這裡仍要冷靜看待:一個候選藥走到 2a 期,代表它開始被看見,不代表它已經完成臨床定論;真正的考驗,還在更長期的療效穩定性與更大規模的人體驗證。

看到 AI Drug Discovery in IPF 這類新聞時,你該怎麼判斷它是真突破,還是只是很會講?
很多人忽略這件事:一則 AI 新藥新聞最迷人的地方,常常不是它真的走了多遠,而是它很會讓你以為終點快到了。真正值得你先看的,不是標題多震撼,而是四個問題。第一,有沒有講清楚靶點是誰,例如 TNIK 這類可被驗證的致病節點。第二,有沒有走到人體試驗,而不只是細胞或動物結果。第三,有沒有交代安全性與功能指標,像 IPF 研究裡常看的 FVC 變化。第四,有沒有把限制講出來,例如樣本數、追蹤時間與後續試驗還沒完成。以 rentosertib 目前的資料來看,它的確已跨過「只存在實驗室」這條線,進入隨機 Phase 2a 人體試驗,這很值得注意;但同時,研究也還沒有大到能直接改寫臨床常規。(nature.com) 你知道嗎?真正成熟的 AI藥物研發,不像神話裡一匙仙丹,比較像把煎藥的火候抓得更準:少一分不熟,多一分會焦。科技能幫我們更快靠近答案,卻不能代替醫學把每一步都走完。

結論:當科技開始把答案拉近病人
有些進步,不是一下子把疾病從世界上抹去,而是先把原本看不清的路,慢慢拉近到病人面前。AI 藥物研發之所以值得注意,不只是因為它讓特發性肺纖維化這類難治疾病多了一個新名字,而是它真的把「找靶點、選分子、進臨床」這條路往前推了一段。從西醫臨床的角度看,真正有價值的,不是新聞說得多震撼,而是證據走到哪裡。像 rentosertib 這樣的案例,之所以值得被記住,不只是因為它和 AI 有關,而是因為它已進入 Phase 2a 人體試驗;而臨床試驗的邏輯本來就很清楚,Phase 1 主要看安全性、劑量與副作用,Phase 2 則開始檢驗治療是否對特定疾病有作用,同時持續補足安全性資訊。這代表它不是終點,但也已經不是只停在實驗室裡的想像。
你現在就可以先做兩件事。第一,當你下次再看到「AI 找到新藥」「AI 改寫醫療」這類標題時,先別急著被震住。你可以這樣問自己:有沒有明確靶點?有沒有人體試驗?改善的是機轉、數值,還是病人真正感受到的功能? 第二,如果你或家人正面對慢性肺病、纖維化,或需要長期追蹤的疾病,下次門診時也可以這樣問醫師:「目前這個治療是在壓症狀,還是在改變病程?」、「有沒有新的臨床試驗或研究方向值得追蹤?」 很多時候,問得更準,本身就是照護的一部分。
再往下看一層,多數人容易只記住一句話:AI 讓新藥變快了。其實更值得記住的是,AI 可能讓醫學少走一些錯路。速度只是表面,真正被改變的是排序能力:哪些靶點值得追,哪些分子值得做,哪些結果值得繼續投進人體研究。再深一層,這也提醒我們,未來醫療的競爭不只是誰比較快,而是誰比較能把「早期機轉辨識、臨床可驗證性、病人真正受益」連成一條線。
所以啊,別急著把 AI 想成神話,也別太快把它當成噱頭。它比較像把臨床研究的焦距調得更清楚:原本模糊的東西,開始有輪廓;原本很遠的可能,開始有了可被追蹤的位置。願你讀完這篇之後,帶走的不只是「AI 很厲害」這個印象,而是一套更穩的判讀方式。也歡迎你把最想追問的下一個問題留給我——《本文將依據最新提問持續更新》
| 比較面向 | 傳統藥物研發 | AI 藥物研發(本篇主題脈絡) | 讀者該怎麼解讀 |
|---|---|---|---|
| 起點邏輯 | 多從既有機轉、文獻累積、研究者假設出發 | 可從大規模資料中更早辨識高價值靶點與候選分子 | 差別不只在快,而是在「先看哪裡」 |
| 靶點辨識 | 常需長時間逐步驗證,容易走很多彎路 | 可整合多組學與疾病網路訊號,較快收斂到關鍵節點,如 TNIK | 真正突破常不是先有藥,而是先找到對的靶點 |
| 分子篩選方式 | 大量試錯、逐輪優化,成本與時間都高 | 先用模型篩掉大量低機率分子,再集中資源做優化 | AI 像先幫忙把海水退掉一半,再開始找針 |
| 前期研發速度 | 通常較慢,從靶點到候選藥物需要多年 | 有機會縮短早期發現到候選藥物的時間 | 速度提升是優勢,但不是成功保證 |
| 在 IPF 的代表案例 | 過去多數藥物偏向延緩惡化,真正新機轉突破有限 | 以 TNIK 為標靶、rentosertib 為候選藥物,已走到人體 Phase 2a | 這是「不只停在實驗室」的重要訊號 |
| 目前證據層級 | 多數藥物需經長時間累積,才逐步改變臨床實務 | 已有前臨床+人體早期試驗,但仍未等於臨床定論 | 有進展,不等於已成常規治療 |
| 人體試驗意義 | 通過人體試驗才算真正跨過關鍵門檻 | Phase 1 重安全性;Phase 2 看初步療效與劑量訊號 | 看到人體試驗,要再問「走到第幾期」 |
| 功能指標判讀 | 需看是否真的改善病人相關結果 | IPF 常看 FVC 等肺功能變化與安全性資料 | 不只看「有沒有變好」,還要看變好了多少、能不能持續 |
| 目前限制 | 耗時、昂貴、失敗率高 | 仍受資料品質、模型偏差、可解釋性與後續臨床驗證限制 | AI 不是魔法,只是把排序能力變強 |
| 對病人的真正意義 | 可能較慢等到新機轉治療進展 | 有機會更早看到值得期待的新方向 | 希望變近了,但還需要時間走完最後幾哩路 |
| 對新聞閱讀者的提醒 | 傳統研發新聞通常較少被神化 | AI 題材容易被包裝成「重大突破」 | 要先問:有沒有靶點?有沒有人體試驗?有沒有功能性結果? |
參考文獻:
- (註1) Pun FW, Ozerov IV, Zhavoronkov A. AI-powered therapeutic target discovery. Trends in Pharmacological Sciences. 2023;44(10):663-675. PubMed
- (註2) Ren F, Aliper A, Chen J, et al. A small-molecule TNIK inhibitor targets fibrosis in preclinical and clinical models. Nature Biotechnology. 2025;43:63-75. Nature
- (註3) Selman M, Buendia-Roldan I, Pardo A. Artificial intelligence in idiopathic pulmonary fibrosis. European Respiratory Journal. 2026;67(1):2501112. ERS Publications
- (註4) Xu Z, Ren F, Wang P, et al. A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine. 2025. Nature Medicine
- (註5) Xu Z, Ren F, Wang P, et al. A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine. 2025 Aug;31(8):2602-2610. Nature Medicine / PubMed
- (註6) Ren F, Aliper A, Chen J, et al. A small-molecule TNIK inhibitor targets fibrosis in preclinical and clinical models. Nature Biotechnology. 2025;43(1):63-75. Nature Biotechnology / PubMed
- (註7) Xu Z, Ren F, Wang P, et al. A generative AI-discovered TNIK inhibitor for idiopathic pulmonary fibrosis: a randomized phase 2a trial. Nature Medicine. 2025 Aug;31(8):2602-2610. Nature Medicine (nature.com)
- (註8) Niazi SK. Artificial intelligence in small-molecule drug discovery: a critical review of methods, applications, and real-world outcomes. Pharmaceuticals. 2025;18(6):847. MDPI (mdpi.com)
文章來源:上醫預防醫學發展協會